原子吸收光譜儀的結構及詳細原理(上)

(上)篇包括原子吸收光譜分析方法的歷史、原子吸收光譜分析的理論基礎以及原子吸收的測量和數據分析。
(下)篇包括原子吸收光譜儀的結構和詳細原理
原子吸收光譜法:被測元素基態原子在蒸汽狀態下,外層電子由基態躍遷至激發態, 對光源發出的原子特征波長光輻射進行吸收, 引起特征波長光輻射的透射光強度減弱。原子吸收光譜法是基于此建立起的元素定量分析的方法,它是測定痕量和超痕量元素的有效方法之一。
棱鏡實驗
1666年,愛思考的牛頓先生發現,太陽光經過棱鏡后被分成了華麗麗的彩色光帶,他把這條光帶稱為光譜。

1802年,Wollaston發現了光譜中的黑線,但沒給出科學的解釋。
1814年,愛觀察的Fraunhofer再次觀察到了太陽光譜中的黑線,他在小黑屋內將一塊火石玻璃棱鏡放置在經緯儀前,讓太陽光通過小縫投射到棱鏡上,用經緯儀上的望遠鏡觀察光譜時看到了很多條黑度不等的黑線密集在光譜上(這大概就是傳說中五彩斑斕的黑)。

其中有兩條最強的緊靠在一起的黑線,用字母D予以標記。他測定未分辨的D線的平均波長為588.7nm,與現在的精確值589.2nm已經非常接近。
Kirchhoff和Bunsen的實驗
真正對原子吸收光譜的產生做出透徹解釋的是后來的Bunsen和Kirchhoff。
他們進行的鈉光譜中譜線自蝕的實驗,是歷史上用原子吸收光譜進行定性分析的第一個例證。
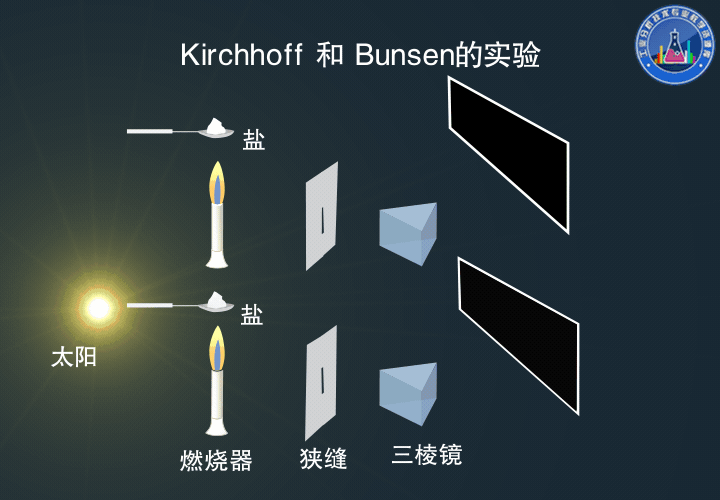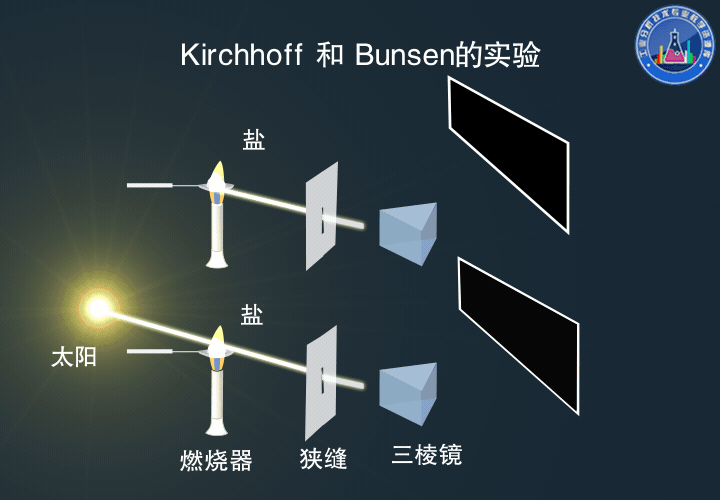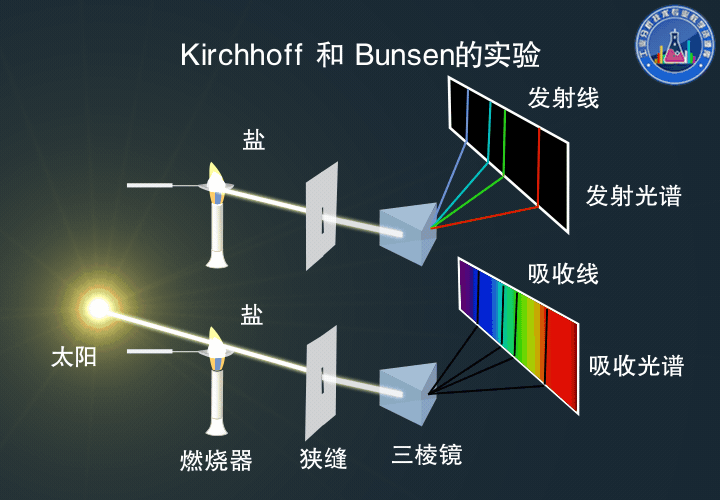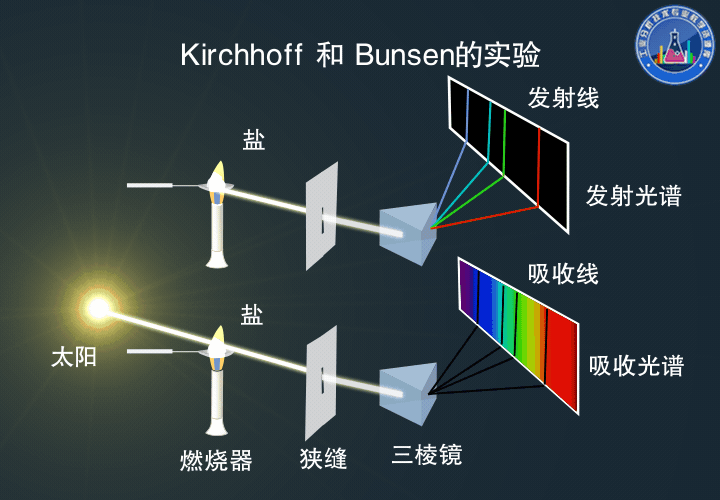
下:光束通過加熱的金屬鹽后,觀察到Fraunhofer吸收線
原子結構
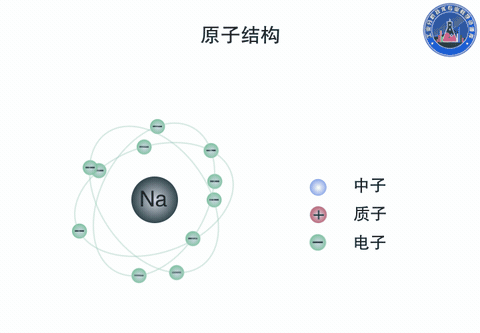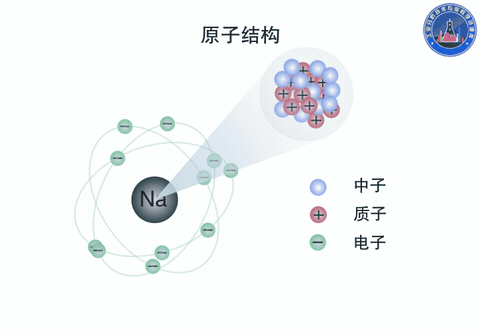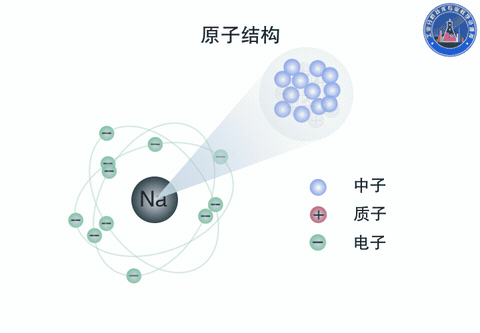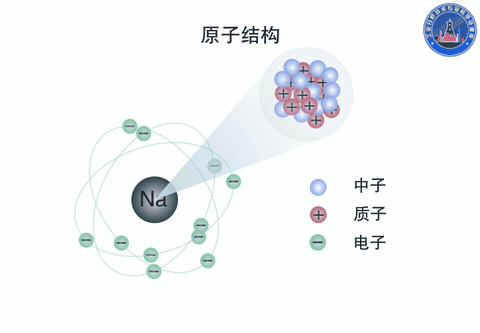
原子由原子核和核外電子組成。原子核是原子的中心體,由質子和中子構成,帶正電。電子帶負電,總的負電荷數與原子核的正電荷數相等。電子沿核外的圓形或橢圓形軌道圍繞著原子核運動,同時又有自旋運動。
原子躍遷和能級圖
電子由于具有不同的能量,就按照各自不同的軌道圍繞原子核運轉,即能量不同的電子處于不同的相應等級。
電子從基態躍遷到能量最低的激發態(稱為第一激發態)時要吸收一定頻率的光,這種譜線稱為共振吸收線;當它再躍遷回基態時,則發射出同樣頻率的光(譜線),這種譜線稱為共振發射線(它們都簡稱共振線)。

原子躍遷和激發
基態原子吸收一定頻率的輻射能量,外層電子由基態躍遷到第一激發態或者更高激發態,產生共振吸收線,生成原子吸收光譜。
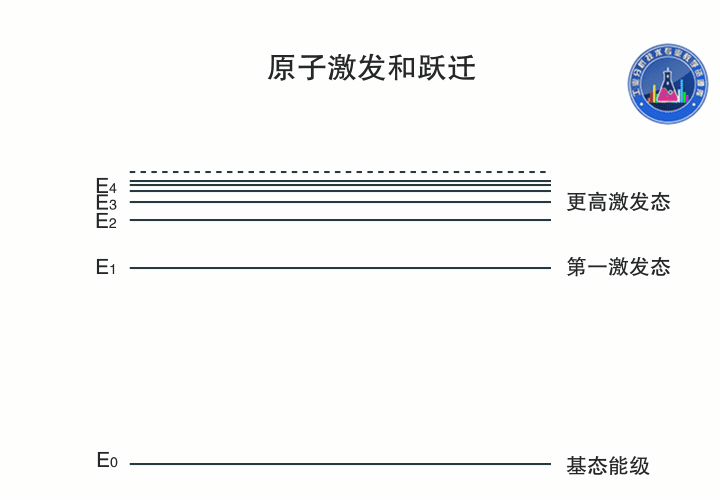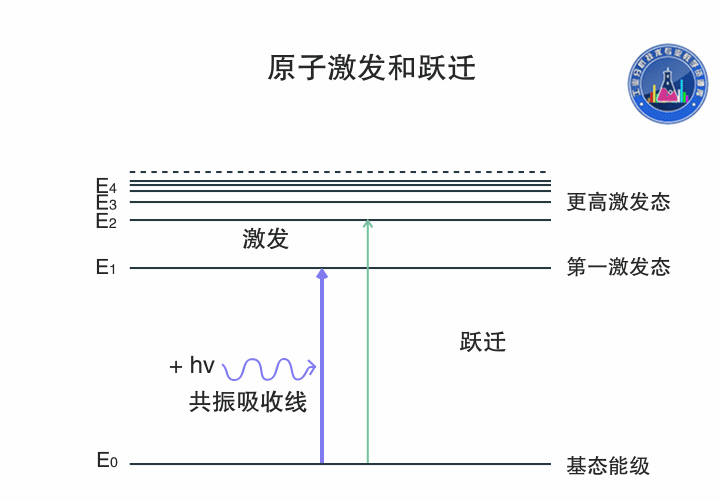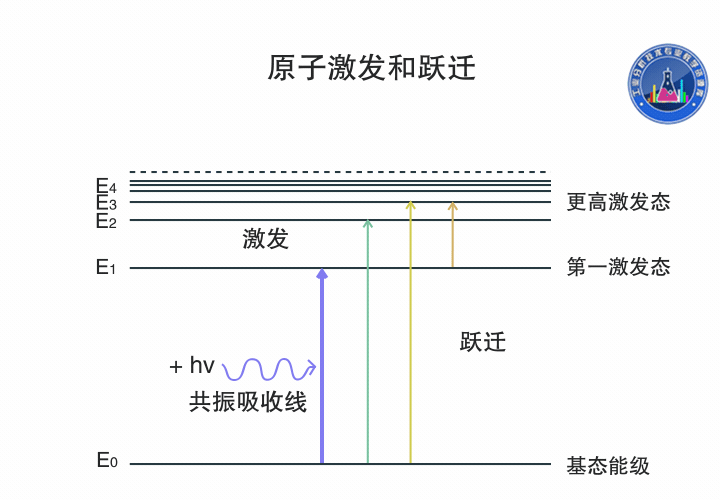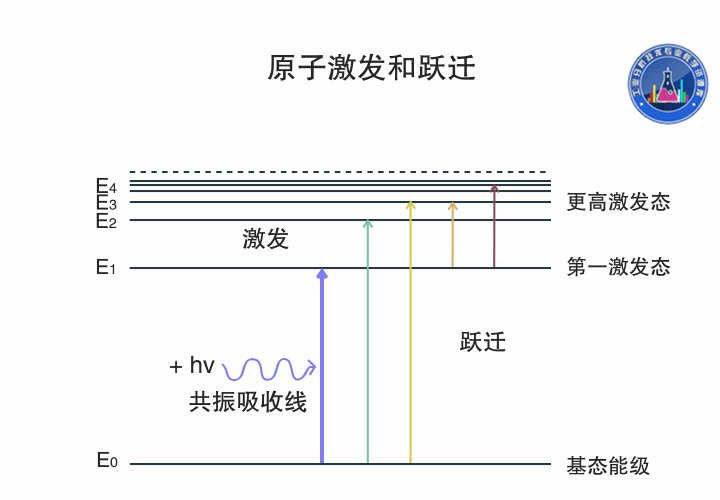
圖中氫原子的電子可以通過吸收不同頻率的輻射能量在各個能級間躍遷。
朗伯-比爾定律
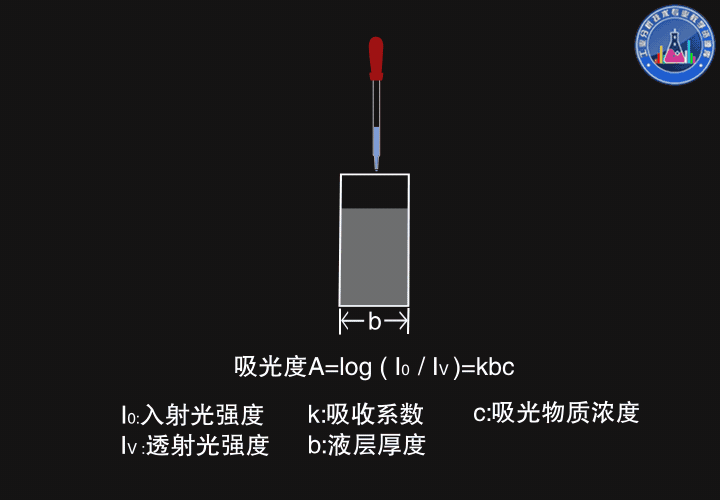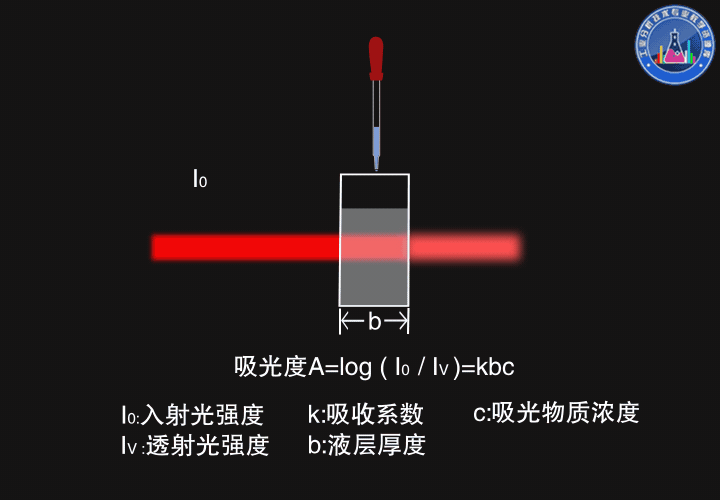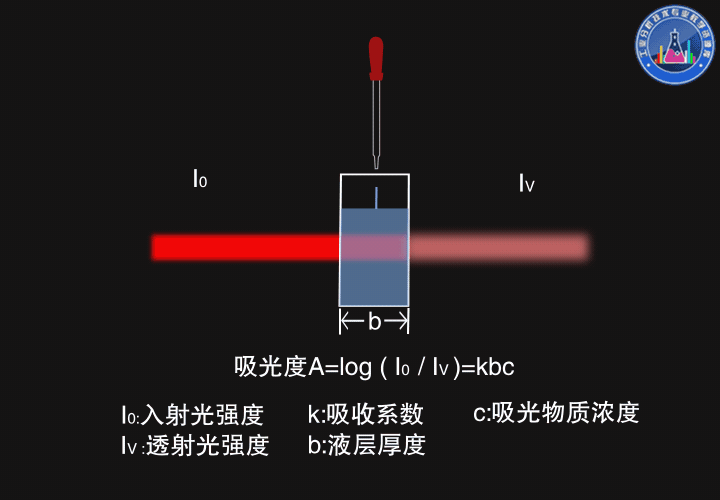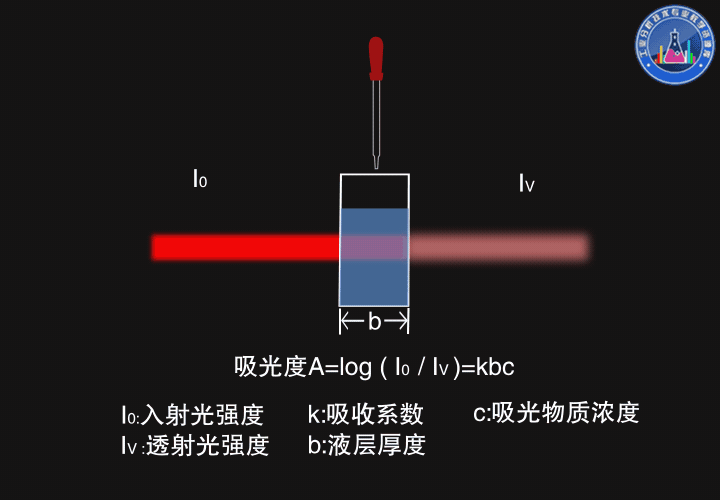
一束強度為I0的光通過厚度為b的原子蒸氣,部分光被吸收,部分光被透過,透射光的強度Iν服從朗伯-比爾定律(Lambert-Beer law),吸光度A=log(I0/Iν)=kbc
如圖所示,厚度變大時,透射光強度變弱,吸光度變大。

當濃度變大時,透射光強度也變弱,吸光度變大。
原子吸收光譜的譜線輪廓
原子結構簡單,理論上應產生線狀光譜吸收線,但實際上用強度為I0的不同頻率輻射光照射時,獲得的是峰形吸收,所得曲線為吸收線輪廓。
原子吸收光譜線占據著相當窄的頻率范圍,有一定的寬度,通常用吸收線的中心頻率或中心波長與吸收線的半寬度來表示吸收線輪廓特征。
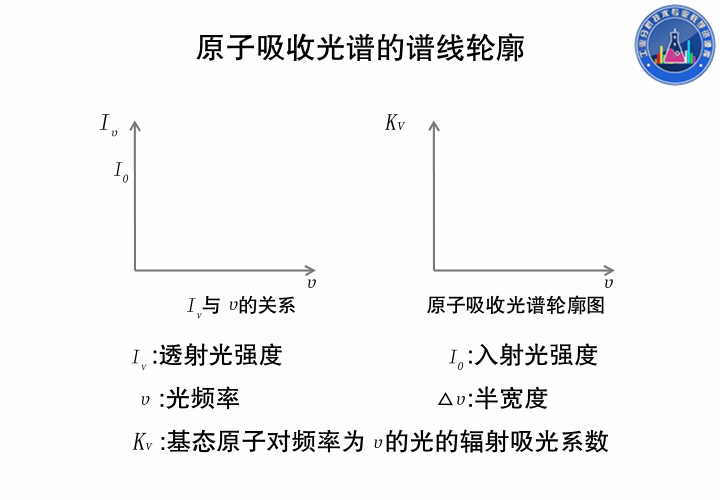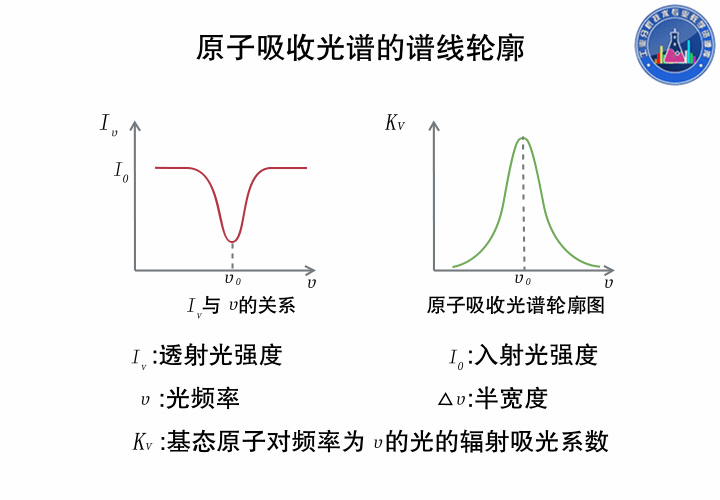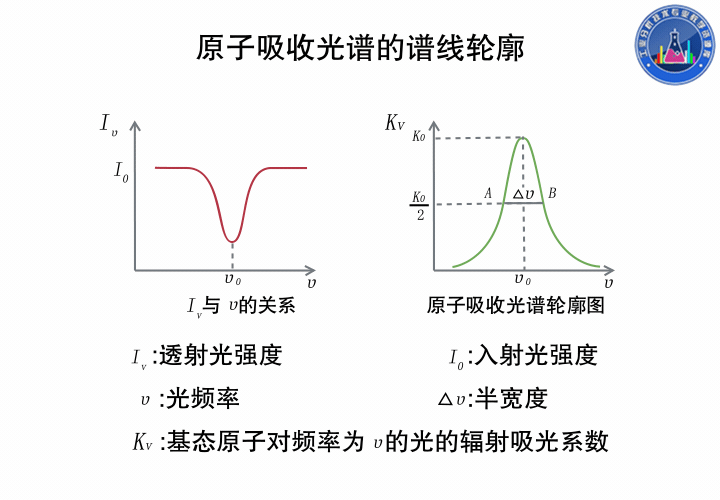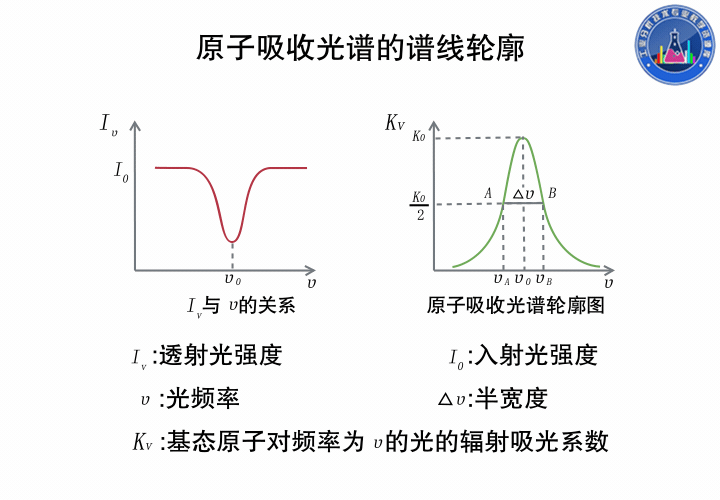
上圖中,左邊是透射光強度和光的頻率的關系,右邊是與之對應Kv與ν的關系。
吸收系數Kv是基態原子對頻率為ν的光的輻射吸收系數,它隨光源的輻射頻率ν而改變,這是由于物質的原子對不同頻率的光的吸收不同。
中心頻率ν0指最大吸收系數對應的頻率,由原子能級決定。
半寬度Δν0是指吸收系數極大值一半處,譜線輪廓上兩點之間頻率(波長)的距離,大約在10-3到10-2nm之間。
積分吸收測量法
在吸收線輪廓內,以吸收系數對頻率積分稱為積分吸收,積分得的結果是吸收線輪廓內的總面積,它表示原子蒸氣吸收的全部能量。
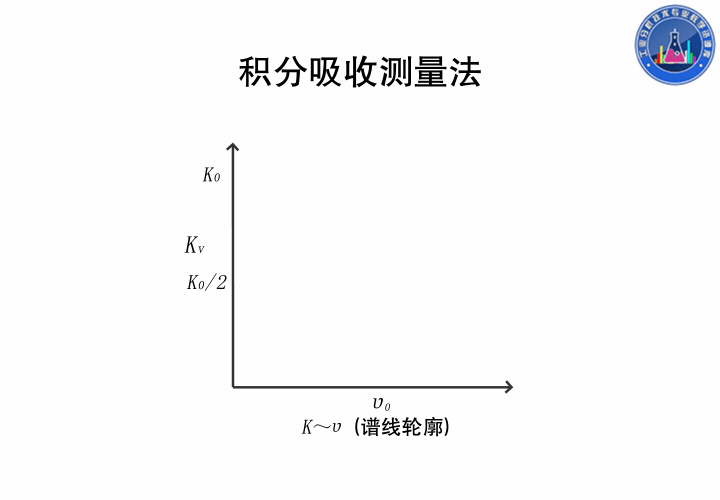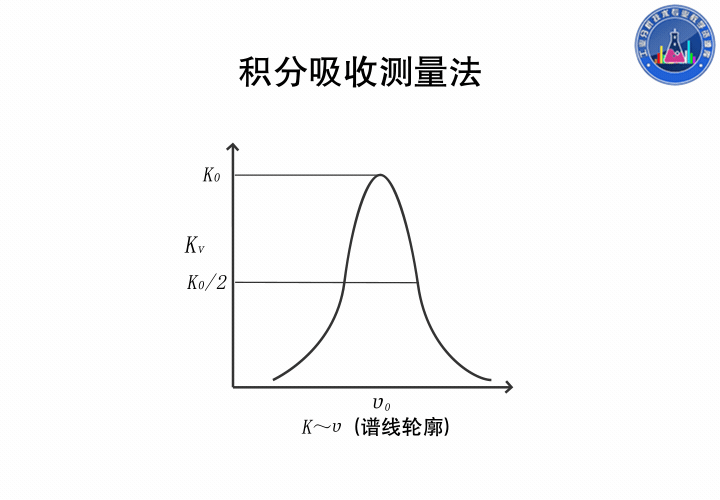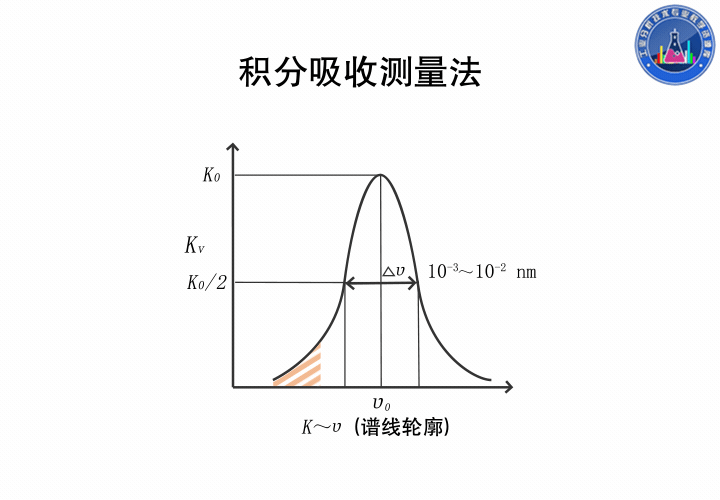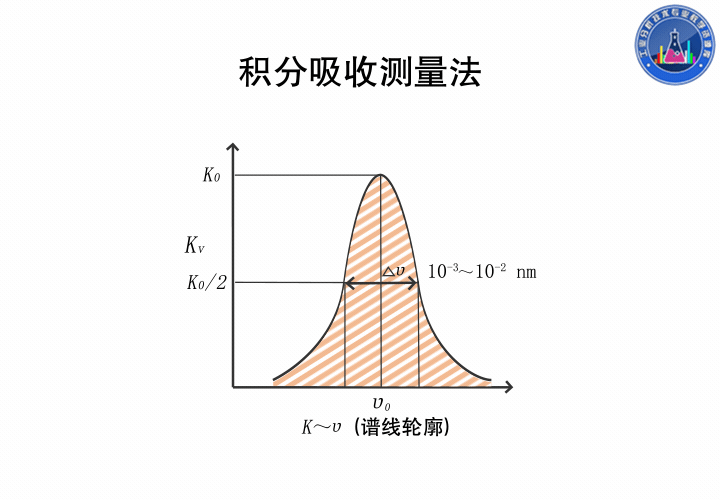
這是一種絕對測量方法,理論上,積分吸收與原子蒸氣中吸收輻射的基態原子數成正比,若能測得積分吸收,就能求出原子濃度,但吸收線半寬度僅為10-3nm,現在的分光裝置無法實現。
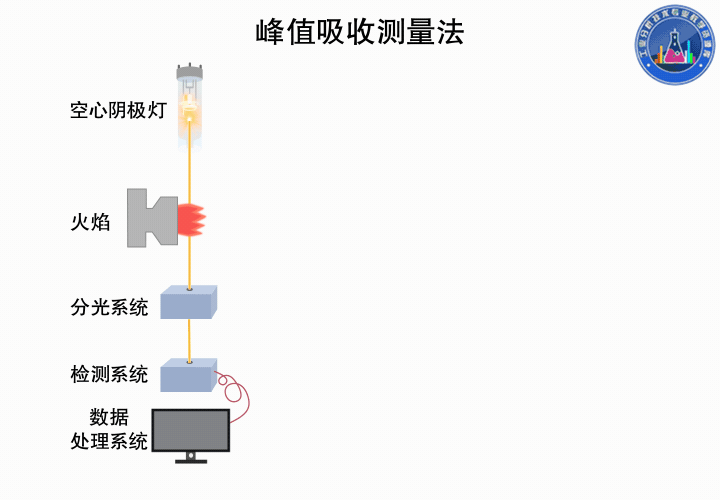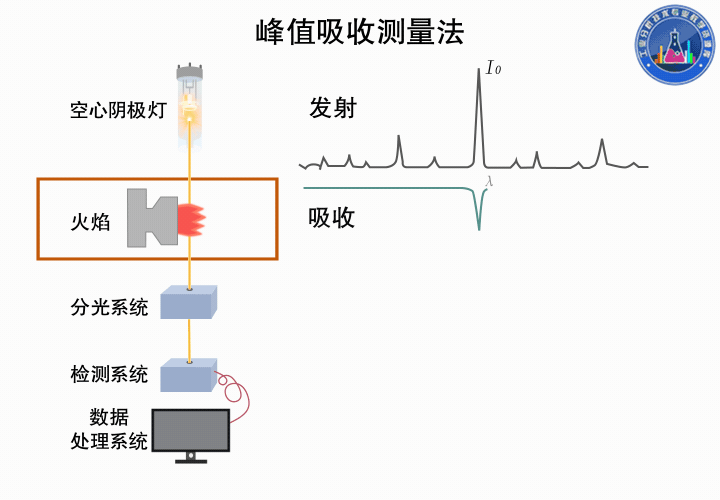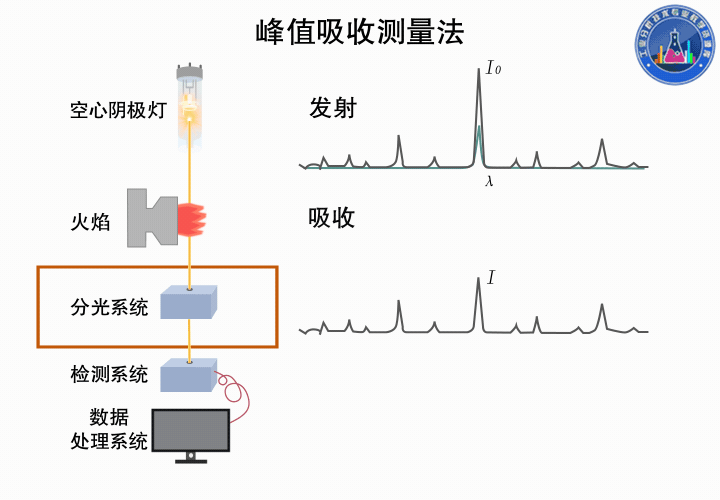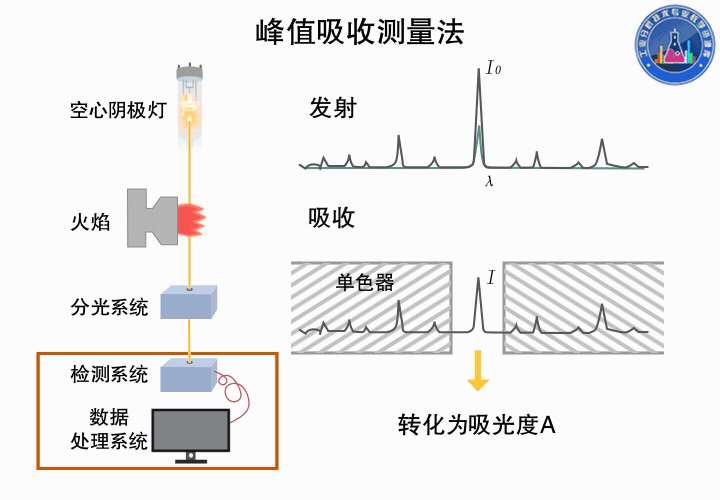
峰值吸收測量法
吸收線中心頻率處的吸收系數Kn為峰值吸收系數,簡稱峰值吸收。
1955年Walsh提出在溫度不太高的穩定火焰條件下,峰值吸收與火焰中被測元素的基態原子濃度也成正比,因此可用峰值吸收代替積分吸收。前提是采用銳線光源,即發射線半寬度比吸收線半寬度小得多的光源(例如空心陰極燈),并且發射線的中心與吸收線中心一致。
下圖所示為峰值吸收測量的過程: